1.定义及流行病学“glaucoma”来源于希腊语“glaukos”,l意思为“淡蓝”、i“蓝灰”,l早在公元前400年的《希波克拉底誓言》中就被提及。然而在此后的几百年中,l它一直被认为是一种晶状体的疾病。对青光眼的正确认识始于对白内障的正确解剖定位,l随后的研究使人们逐渐认识到视神经在青光眼中也被累及。视神经凹陷作为青光眼的一个体征在18世纪50年代后期由解剖学家Heinrich1Muller确认,l青光眼患者视野缩小和旁中心缺损则在1856年由Von1Graefe首先描述。我国早在秦汉时期的《神农本草经》中就有青盲眼病的记载,l但所谓青盲眼病包含了其他一些眼底疾病在内,l直到元明时代才将“青盲”肯定地区别开来,l称绿风内障。现代医学根据患者患病和失明的特征表现将“glaucoma”译为“青光眼”。
青光眼(glaucoma)包含了一大类疾病,l随着对青光眼研究认识的不断深入,l其内涵不断地丰富。一些书籍,l尤其是来自欧洲大陆的,l将具有眼球内压力(intraocular1pressure,lIOP,l眼压)升高共同特点的一组疾病定义为青光眼;在主要来自英语国家的有关文献中,l只是将产生视神经损伤和视功能损害的这类疾病定义为青光眼;而在亚洲,l青光眼的定义除了上述的范畴外,l还包括了具有眼部解剖特征、i可能发生眼压升高的临床前期闭角型青光眼。因此,l我们将青光眼定义为:i一组威胁和损害视神经视觉功能,l主要与病理性眼压升高有关的临床征群或眼病。也就是说如果眼压超过了眼球内组织,l尤其是视网膜视神经所能承受的限度,l将给眼球内各组织(包括角膜、i虹膜和晶状体),l尤其是视神经视功能带来损害,l最典型和最突出的表现是视神经乳头的凹陷性萎缩和视野的特征性缺损缩小。如不及时采取有效的治疗,l视野可以全部丧失,l终至失明。而这种青光眼导致的失明,l就目前的医学技术水平来说是无法使其逆转和恢复的。
流行病学研究资料表明,l青光眼在全球是仅次于白内障的导致视力丧失的主要病因。世界卫生组织及Quigley根据收集的资料推测全球原发性青光眼患者约6680万(2000年),l其中约10%的患者失明。我国的原发性青光眼患病率为0.52%,l50岁以上人群其患病率达2.07%(1996,l北京顺义),l青光眼的致盲率为9.04%(广东新会)~10%(北京顺义)。在发达国家青光眼患者中得到及时诊断治疗的也只有50%左右,l并且治疗中的患眼视功能每年仍有部分继续恶化。因此,l广泛、i深入地开展青光眼的流行病学研究对找寻可能的发病因素,l包括遗传学规律、i致病基因筛查和环境、i精神因素的影响,l以及视神经视功能损害的相关危险因素等,l均有重要的现实意义。青光眼的防盲工作也必须建立在科学地掌握其发生发展规律,l早期诊断和早期治疗的基础上。
2.青光眼性视神经病变及其病理基础11青光眼中最核心的问题是视神经病变,l因为无论是哪一类的青光眼,l都具有共同的视网膜视神经损害这一病理结局。青光眼视神经损害临床上表现为特征性的视神经萎缩,l是神经节细胞轴突变性的直接表现。视网膜神经节细胞损伤变性,l最终死亡的方式是凋亡。
与青光眼密切相关的是视神经的眼内段,l即从视盘表面开始,l穿过巩膜筛板(scleral1lamina1cribrosa)出眼球,l长约1mm。通常称视神经乳头(optic1nerve1head),l由视网膜神经节细胞(ganglion1cells)的轴突、i神经胶质细胞、i胶原支架组织和血管组成。视网膜神经节细胞分为M细胞和P细胞,l前者轴突较粗大,l司暗视觉,l后者轴突较小,l司色觉和分辨觉。神经节细胞的轴突由星形胶质细胞分隔成束状,l以水平线为界,l呈弓形排列分别从上、i下方汇集入视盘(图12-1)。
青光眼视野损害的形态与神经轴突的排列相对应。组织病理研究表明早期青光眼的改变是筛板层的神经轴突、i血管和胶原细胞丧失,l形成青光眼性杯凹,l伴筛板板片结构的压缩和融合,l尤其在视盘的上、i下极更为明显,l因为视盘的上、i下极神经纤维最密集,l是青光眼的易损部位。临床上视盘的改变可早于目前已有的视野检查设备所检出的视野损害。随着病程进展,l组织结构的改变扩张到筛板后区,l筛板弓状后凹,l视神经乳头最终呈盂状凹陷。儿童青光眼的杯凹伴有整个巩膜环的扩张,l同时,l在眼压控制后具有一定的可逆性改变,l因此视神经乳头杯凹形态变化较大。
图12-111视网膜神经纤维汇入视盘
造成青光眼视神经损害的主要因素是升高的眼压,l同时也存在一些易感因素如近视眼,l糖尿病和心血管疾病等。传统上有两种理论:i机械压力学说和血管缺血学说。机械学说强调眼压作用于筛板直接压迫视神经纤维,l阻碍了轴浆流运输。血管学说则强调眼压对视神经血管的影响作用。目前认为是机械压迫和血供障碍共同参与了青光眼视神经损害,l伴随着眼压的升高,l视网膜视神经血管的自我调节机制障碍,l可能促成了视神经的损害。此外,l还存在青光眼类型(如闭角型青光眼、i发育性青光眼主要是高眼压造成视神经损害)和个体间的差异。近年来又提出了青光眼视神经损害的自身免疫病理机制新学说。
参与青光眼性眼部组织损伤的因素可以简要地概括如下:i①眼压对神经元、i筛板、i结缔组织、i血管和角膜内皮细胞等的机械性压迫损伤。②代谢物质的剥夺:i继发于轴浆流的机械性阻断和(或)遗传因素使神经生长因子不足等导致的神经营养因子缺乏;以及视网膜和脉络膜血管自身调节异常、i循环灌注减少、i氧运输异常等造成的缺血缺氧。③异常的胶质细胞、i神经元、i结缔组织等自身免疫缺陷。④一氧化氮合成酶不足或被抑制、i热休克蛋白异常等保护机制的缺陷。⑤谷氨酸对视网膜神经节细胞和其他组织的毒性作用。⑥遗传易感性,l包括大筛孔、i异常结缔组织和异常血管等视乳头结构,l以及小梁网细胞外间质通透性降低、i内皮细胞异常等房水外流系统。⑦分子生物学方面的异常,l如存在异常的TIGR、iOPTN基因等。
青光眼视神经病变的发生大多数与眼压的病理性升高有关。眼压是眼球内容物作用于眼球壁的压力。统计学上的正常眼压值(均值±2个标准差)是11~21mmHg,l代表95%正常人群的生理性眼压范围。正常眼压的生理作用在于保持眼球固有形态、i恒定角膜曲率、i保证眼内液体正常循环以及维持屈光间质的透明性,l这对视觉功能有着重要的意义。由于眼球容量是固定的,l因此构成眼球内容物的晶状体、i玻璃体、i眼内血液量及房水的改变必然伴随眼压的变化。而通常前三者的变化不大,l唯有房水循环的动态平衡直接影响到眼压的稳定性。房水循环途径中任何一个环节发生障碍,l都会影响到房水生成与排出之间的平衡,l表现为眼压的高低变化。青光眼中眼压升高的病理生理过程主要有三个方面:i睫状突生成房水的速率增加,l房水通过小梁网路径流出的阻力增加,l以及表层巩膜的静脉压增加。绝大部分青光眼是因房水外流阻力增加所致。
针对青光眼的上述可能病因机制,l目前临床上的有效措施就是采用各种方法,l使被扰乱的房水循环重新恢复平衡,l控制病理性眼压,l达到每个个体的安全靶眼压水平,l阻止和预防视神经的损害,l保护视功能。降低眼压是目前惟一经证实的青光眼有效治疗方法。相信随着研究认识的不断深入,l繁杂的青光眼视神经损伤过程将会逐渐明了,l针对性的防治措施也将应运而生。
3.青光眼的相关基因研究11青光眼的家族聚集性早已被临床所关注,l大量的家系调查发现青光眼属于多因素疾病,l青光眼是具有遗传倾向性的眼病也已得到国内外学者的公认。目前青光眼的分子遗传学研究成为眼科学和遗传学领域的一个热点。近年来,l随着分子生物学技术的迅猛发展以及人类基因组计划的顺利实施,l青光眼相关致病基因的研究也取得了较大的进展,l先后定位并克隆了不少相关基因(见下表)。但青光眼的发病和遗传方式非常复杂,l涉及到多种基因相互作用以及基因与环境之间的相互作用。尽管已经得到一些青光眼相关致病基因,l还有许多问题亟待解决,l如基因功能特性的研究,l致病基因突变的意义,l相应编码的蛋白质空间结构和相应的功能改变,l与其他基因的相互关系,l是否引起青光眼相关的病理生理改变等等。青光眼相关致病基因的研究使我们能够从基因水平重新认识青光眼的发病机制,l有可能在临床出现青光眼特征性损害前从基因水平作出早期诊断,l对治疗效果和预后作出相应评价,l并为进一步的青光眼治疗方法革新如基因修正或导入外源性正常基因等基因治疗,l最终达到根治青光眼而奠定基础。
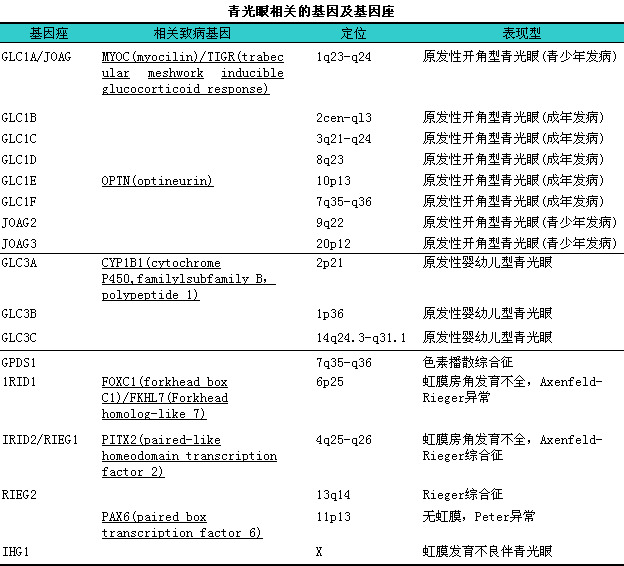
4.青光眼的分类11根据病因学、i解剖学和发病机制等,l青光眼有许多种分类方法,l临床上通常将青光眼分为原发性、i继发性和发育性三大类:i
(1)原发性青光眼(primary1glaucoma):i这类青光眼的病因机制经过长期的研究,l逐步了解但尚未完全阐明,l为与继发性青光眼相区别,l习惯上仍称为原发性青光眼,l是主要的青光眼类型,l在我国约占86.7%,l发生在成年以后人群。
(2)继发性青光眼(secondary1glaucoma):i由眼部其它疾病或全身疾病等明确病因所致的一类青光眼,l可见于各年龄人群。
(3)发育性青光眼(developmental1glaucoma):i为眼球在胚胎期和发育期内房角结构发育不良或发育异常所致的一类青光眼,l于婴幼儿和青少年时期发病。