一、i疾病概述
慢性炎性脱髓鞘性多发性神经病(chronic1inflammatory1demyelinating1poiyneuropathy,lCIDP)是由免疫介导的感觉、i运动性周围神经脱髓鞘性疾病。其特点为起病缓慢、i复发病程或进行性病程,l其临床病理改变与急性炎性脱髓鞘性多发性神经病相似。1921年Mattrass根据其临床病理改变将本病命名为“复发性肥大性神经炎”,l此后相继出现许多不同命名:i慢性复发性炎性神经病(chronic1relapsing1inflammatory1neuropathy,lCRIN)、i慢性炎性多发性周围神经病(chronic1inflammatory1polyneuropathy,lCIP)、i慢性炎性脱髓鞘性多发性神经病(ehro-nic1inflanmmtory1demyelinating1polyneuropathy,lCIDP)。
【病因及发病机制】
本病确切病因尚不清楚。在CIDP中自我耐受性崩溃,l自身反应性T细胞和B细胞活化,l引起以自身免疫性疾病为特征的器官特异性损害。分子模拟概念可能与自身免疫性神经病的耐受性崩溃特别相关。可能与以下几点有关。
1.遗传易感性HLA相关基因为Aw30、iAw31、iDRw3、iDw3。
2.细胞免疫异常 CIDP患者系统免疫T细胞活化,l经黏附分子、i趋化因子和基质金属蛋白酶的作用,l在血液神经屏障失调情况下,l移行穿越血液一神经屏障,l入侵周围神经组织。在周围神经系统内,l受MHC分子中相应的提呈抗原和共刺激信号作用发生克隆扩张,l表达和分泌细胞因子,l如肿瘤坏死因子-α(TNF-α)、iγ-干扰素(IFN-γ)和白介素2(IL-2)。并激活巨噬细胞释放具有神经毒性和激发免疫反应的分子(即氧自由基、i一氧化氮代谢产物、i花生四烯酸代谢产物、i蛋白酶和补体成分),l或增强对髓鞘或神经鞘细胞的吞噬活性和细胞毒活性。此外,l巨噬细胞还起抗原提呈细胞的作用,l调节局部免疫反应和疾病的临床病程。
3.体液免疫异常11自身抗体对CIDP发病机制也起作用,l有髓鞘神经纤维上沉积免疫球蛋白和补体以及脑脊液存在寡克隆IgG带都是异常体液免疫的佐证。被动转移CIDP,1患者血清或纯化IgG,l可诱导大鼠神经的传导阻滞和脱髓鞘。此外,l脱髓鞘和传导阻滞也可能由以髓鞘为作用目标的抗体以外的血清成分引起,l如细胞因子、i补体或其他炎性介质(如一氧化氮)。部分CIDP患者近期发生空肠弯曲杆菌感染,l而神经糖脂与微生物脂多糖具有相同的糖类抗原决定簇,l提示分子模拟是罕见情况下CIDP的基础病因。
4.轴突消失CIDP虽然是一种脱髓鞘性多神经病,l但也与轴突消失相关,l而且ClDP的远期预后取决于轴突消失而不是脱髓鞘的程度。对于神经毒细胞因子(如TNF-α)和有害介质(例如一氧化氮和金属蛋白酶)的释放是否增强轴突破坏尚有疑问,l但是现在越来越清楚,l早期有效治疗可以最大程度地减少轴突消失。
【临床表现】
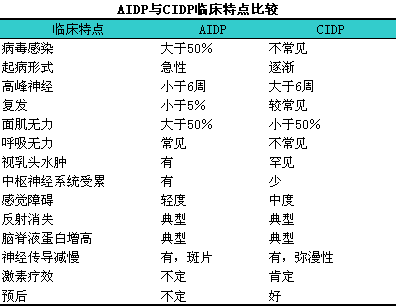
本病发生于任何年龄,l以中青年多见(40岁~60岁)。男性比女性多。大多数患者发病前无呼吸道、i胃肠道感染等前驱症状或诱因。亚急性或慢性起病,l常难以叙述确切发病时间。多数患者缓慢加重。以运动障碍为主,l且有明显的肌肉萎缩,l以双下肢无力为首发,l并逐渐向上肢发展。近端重于远端,l常为对称性。肌张力减退,l腱反射消失,l无病理反射。一般无呼吸肌受累。深浅感觉均有障碍,l如肢体麻木、i刺痛、i紧束或疼痛感,l检查可发现感觉呈袜套样分布,l严重者有感觉性共济失调。自主神经性营养障碍明显,l如口眼燥,l皮肤灼热感,l干燥而无汗,l脱屑、i色素沉着及浮肿。个别患者有血压不稳。无大小便障碍。约10%患者有尺神经、i耳大神经及腓肠神经等神经肥大。CIDP的症状体征与急性炎性脱髓鞘性多发性神经病(A1DP)相似,l但变异较大,l两者比较见下表。
临床分型根据不同病程可分为4型:i①复发型占34%,l反复加重性发展,l部分有缓解;②阶梯式进行型占34%,l在逐渐发展的基础上,l间断地加重无缓解;③缓慢单相型占15%,l病情逐渐加重至一定程度后不再加重,l但病情加重的病程至少持续6月以上;④缓慢进展型占15%,l病情无限制地逐渐加重,l直至患者卧床不起。
【诊断和鉴别诊断】
慢性进行性的对称性肢体无力及感觉障碍,l腱反射减退或消失,l脑脊液蛋白增高而细胞数正常,l肌电图示神经性受损,l排除其他可能引起周围神经病的原因即可诊断。目前国际上较多采用Pentland诊断标准:i①以运动障碍为主的多发性神经病变,l倾向于近端损害,l但也可损害远端;②病程呈持续进展,l或缓解复发历时六个月以上;③脑脊液细胞蛋白分离;④电生理示周围性神经源性损害(脱髓鞘、i轴索变性);⑤除病前或病之初期可有短时间的炎症表现外,l不伴其他全身性疾病;⑥血、i尿、i粪常规,l血钙、i磷,l免疫球蛋白,l肝功能及尿卟啉均正常;⑦神经病理示慢性炎性脱髓鞘性神经病以及葱头样肥大眭神经特征。
本病应与下列疾病相鉴别:i
1.其他原因引起的继发性周围神经病 许多原因可引起缓慢发展的周围神经病,l具有与CIDP相似的临床表现。这主要是进行相关病因的排除,l周围神经病常见病因有糖尿病、i慢性酒精中毒、i营养障碍、i遗传、i环境毒物和药物、i风湿性、i胶原血管性、i淀粉样变、i副癌综合征、i全身疾病等,l这些原因引起的周围神经病脑脊液蛋白含量往往正常。
2.遗传性感觉运动性神经病 本病有遗传家族史,l自幼发病,l病史长,l多伴有其他畸形,l脑脊液蛋白含量无增高,l偶可发现有多脏器与多系统损害。对皮质类固醇治疗反应差。
3.多灶性运动(感觉)神经病(Lewis-Summer1syndrome)肢体肌无力为非对称性,l远端重于近端;可有感觉障碍,l但一般不严重。肌电图示神经远端潜伏期长,l神经传导速度减慢,l多灶性传导阻滞,l脑脊液蛋白含量增高。神经活检提示神经髓鞘脱失,l轴索呈束性丧失。
4.局灶性上肢脱髓鞘性神经病(Thomas病)11可累及单侧或双侧肢体,l可以是感觉神经、i运动神经或感觉与运动神经均受损,l早期主要表现为感觉异常或麻术。血清抗神经节苷脂GMI抗体多为阴性。对皮质类同醇治疗反应好。
二、i检验诊断
脑脊液蛋白细胞分离现象是诊断CIDP的重要佐证,l血清脑脊液免疫参数可对部分AIDP的诊断、i预后及病情判断起帮助作用。一些患者可能需要更广泛的实验室检查,l以查找导致CIDP的其他原因和并发疾病。
【一般检验项目】
1.脑脊液细胞学及蛋白定量 详见本章第一节“多发性神经病”。为CIDP的实验室检查必须项目。脑脊液可见蛋白细胞分离,l但蛋白量波动较大。蛋白增高,l特别在复发期蛋白含量常在0.8g/L~2.5g/L,l有的高达9.5g/L。病情严重程度与蛋白量有关。偶有患者在正常范围内,l较罕见。CIDP患者脑脊液蛋白增高达高峰时间长。血清HIV阴性时,l细胞数<10/μl,l血清HIV阳性时,l细胞数<50/μl。
2.脑脊液蛋白电泳11详见本章第一节“多发性神经病”。CIDP、i神经梅毒(nerve1syphilis)脑脊液γ球蛋白多增高。少数CIDP患者脑脊液γ球蛋白可高于160mg/L。
31.CSF寡克隆区带(OCB)部分患者可出现OCB阳性。详见本章第二节“急性炎性脱髓鞘性多发性神经病”。
【特殊检验项目】
1.抗神经节苷脂抗体
(1)检测方法:iELISA、i欧蒙印迹法。
(2)标本:i血清、i脑脊液。
(3)参考范围:i正常人阴性。
(4)临床诊断价值和评价:i神经节苷脂(GM)是一种髓鞘成分,l它存在于神经元表面,l调节多种生理过程,l如参与细胞识别、i细胞粘附,l并与生长因子受体及离子通道反应,l从而参与信号传递。它包括多种组分,l在人脑中主要有四类神经节苷脂,l分别是GMI、iGD1a、iGD1b和GT1b。在一些自身免疫性神经病中,l抗GM抗体效价升高与疾病直接相关,l因而测量这些抗体的水平被用来跟踪疾病的康复和发展。在AIDP、iCIDP、i多灶性运动神经病变等周围神经病变患者中可检出抗GM抗体。抗GMIgG和IgM类抗体对外周神经病变具有很高的诊断价值。GMI是神经胞膜最丰富的神经节苷脂之一,l它具有抗原性,l故血清中GMI抗体检测是观察神经损害,l推测其损害机制的一个比较理想的指标。
2.微管蛋白抗体(tubulin抗体)
(1)检测方法:iELISA法。
(2)标本:i血清、i脑脊液。
(3)参考范围:i正常人阴性。
(4)临床诊断价值和评价:itubulin即微管蛋白,l是细胞的一种骨架蛋白。高滴度(1:i11000)的抗β-tubulin抗体的出现,l对CIDP的诊断具有特别意义。
3.抗硫脂(sulfafide)抗体
(1)检测方法:iELISA法
(2)标本:i血清、i脑脊液。
(3)参考范围:i正常人阴性。
(4)临床诊断价值和评价;硫脂是髓鞘膜上含硫酸残基的酸性糖脂,l参与神经鞘膜的构成并与神经鞘膜生理功能密切相关。一些CIDP患者血清中可检测到高滴度的抗硫脂抗体,lCSF中抗硫脂抗体阳性率明显高于血清,l硫脂被认为是以感觉障碍为主的周围神经病的自身抗原。CIDP患者CSF中抗硫脂抗体(IgM)可作为感觉轴索型CIDP的临床辅助参考指标,l抗硫脂抗体的水平与疾病的临床严重程度及预后无明显关系。
4.抗GD1a抗体
(1)检测方法:iELISA法。
(2)标本:i血清、i脑脊液。
(3)参考范围:i阴性。
(4)临床诊断价值和评价;在临床诊断的特发性多发性周围神经病中,l目前发现许多为抗糖脂抗体相关性神经病,l其中运动性神经病包括多灶性运动神经病、iAIDP及肌萎缩侧索硬化症,l抗GMl抗体和抗GD1a抗体检出率较高;AMAN患者和抗GDla抗体的临床相关性比抗GM1抗体更高。
5.抗GQ1b抗体
(1)检测方法:iELlSA法。
(2)标本:i血清。
(3)参考范围:i阴性。
(4)临床诊断价值和评价:i90%以上的Miller-Fisher综合征患者血清中可测得高量的抗GQ1b抗体。和抗GM1抗体不同的是,l抗GQ1b抗体的特异性很高,l较抗GMl抗体更具有诊断上的价值。
【应用建议】
l.1CIDP首选检验项目:i脑脊液常规+蛋白电泳。
2.其他参照项目临床诊断价值和评价合理选取。